烟台海岸带所概述通过代谢重编程突破细菌持留菌休眠屏障的新兴策略
抗生素耐药已成为全球公共卫生和养殖业的重大挑战,即使在使用高浓度抗生素时,仍有部分细菌能短暂存活并导致感染复发。近日,中国科学院烟台海岸带研究所动物资源与活性成分挖掘利用研究组(王义鹏研究团队)总结持留菌代谢调控领域最新进展,系统阐明外源性代谢物如何通过重编程细菌代谢逆转其抗生素耐受性,为解决耐药难题提供全新治疗思路。
细菌持留菌:抗生素杀不死的“休眠杀手”
不同于通过基因突变产生耐药性的细菌,持留菌是细菌群体中天然存在的 “休眠个体”,它们通过降低代谢活性、停止生长繁殖,让依赖活跃代谢靶点的抗生素“无的放矢”。这类细菌广泛存在于大肠杆菌、金黄色葡萄球菌、铜绿假单胞菌、结核分枝杆菌等常见致病菌中,尤其在生物膜内部大量聚集。
研究发现,临床上许多感染病例中分离出的细菌基因型与初次感染完全一致,这说明持留菌在抗生素治疗中存活下来,一旦环境适宜就会重新繁殖。其形成受多重机制调控:毒素-抗毒素(Toxin-Antitoxin,TA)系统会快速抑制蛋白质合成与 DNA 复制,严谨反应磷酸鸟苷[(p)ppGpp]信号通路则像“代谢刹车”,降低细菌能量消耗,而活性氧(Reactive oxygen species,ROS)应激与群体感应(Quorum sensing,QS)系统进一步协同,将细菌推入深度休眠状态。
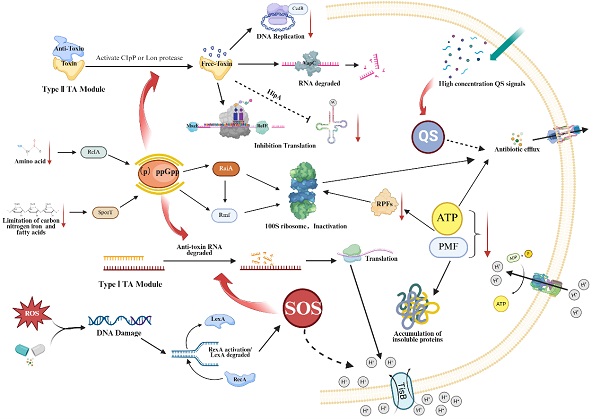
图1 控制持留菌形成的综合调控网络
代谢“唤醒”策略:让休眠菌“主动”对抗生素敏感
既然持留菌的耐药性源于“代谢休眠”,能否通过“唤醒”代谢使其重新对抗生素敏感?本研究重点整理了近年来通过外源代谢物逆转持留菌低代谢状态这一策略的研究进展与分子实例,证实外源性代谢物可精准激活持留菌的核心代谢通路,打破其休眠状态。
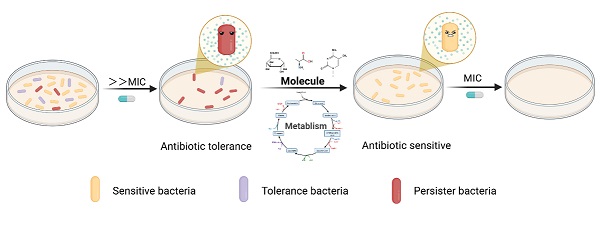
图2 代谢调节可恢复细菌持久性中的抗生素敏感性
在碳代谢物中,葡萄糖、丙酮酸等常见碳源能显著提升氨基糖苷类抗生素对大肠杆菌持留菌的杀伤效果。这些代谢物能激活糖酵解和三羧酸循环,增加还原型烟酰胺腺嘌呤二核苷酸(Nicotinamide adenine dinucleotide,NADH)生成,进而恢复细菌细胞膜的质子动力势(Proton motive force,PMF)— 这是氨基糖苷类抗生素进入细菌内部的关键“通道”。
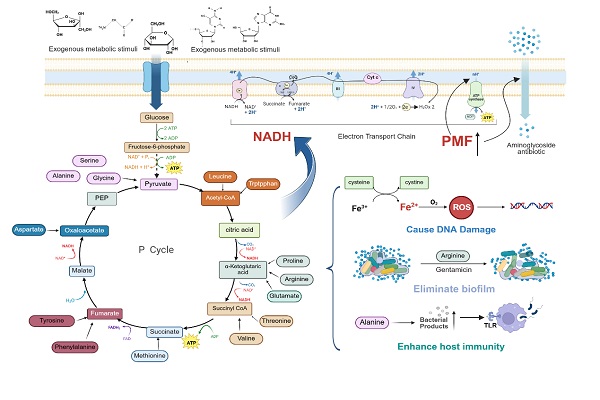
图3 糖和脂重新激活持留菌中枢代谢、增强抗生素疗效和免疫清除率
氨基酸代谢物作用同样显著。例如,丙氨酸可通过丙酮酸循环提升细菌内ROS水平,增强氟喹诺酮类抗生素的DNA损伤效应;L-精氨酸不仅能在碱性环境中强化膜电位,还能破坏生物膜结构,使深藏其中的持留菌暴露在抗生素作用下。
此外,脂质代谢物(如,顺式-2-癸烯酸)可通过调控群体感应信号,抑制生物膜形成;核苷酸代谢物(如腺苷、尿嘧啶)则能激活嘌呤 / 嘧啶拯救通路,恢复持留菌的腺苷三磷酸(ATP)水平与蛋白质合成,使其重新成为抗生素的靶点。
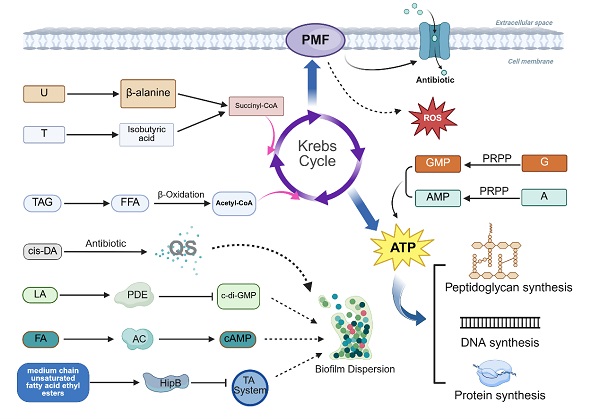
图4 脂质和核苷酸衍生的代谢物恢复能量代谢并破坏生物膜、使持留菌对抗生素敏感
破解耐药难题:为临床治疗提供新方向
当前,临床对抗持留菌主要依赖长期大剂量使用抗生素,这不仅易引发副作用,还会加速耐药基因突变。而“代谢重编程 + 抗生素”联合策略,具有三大优势:一是利用人体自身存在的天然代谢物(如葡萄糖、丙氨酸),安全性高、副作用小;二是不直接杀灭细菌,而是通过“唤醒”增强现有抗生素疗效,降低其耐药性进化风险;三是适用范围广,已在革兰氏阳性菌(如金黄色葡萄球菌)、革兰氏阴性菌(如大肠杆菌、铜绿假单胞菌)中验证有效。
此外,本研究还讨论了外源代谢物从基础研究到临床转化所面临的挑战,包括体内递送、毒性评估、生态学影响与规模化生产等,并建议未来研究需联合药物化学、药剂学与药理学,开展跨学科攻关以推动临床验证。
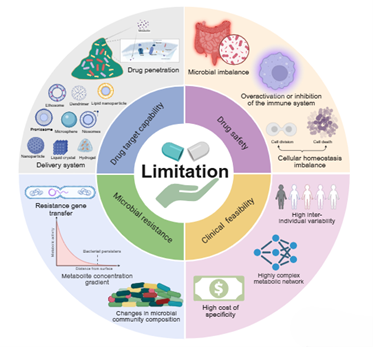
图5 基于代谢物的抗菌佐剂临床转化的主要局限性和挑战
相关成果以“Metabolite-driven reprogramming of bacterial persisters: Mechanisms and therapeutic opportunities for overcoming antibiotic tolerance”为题发表于国际耐药研究领域权威期刊《Drug Resistance Updates》(IF=21.7),烟台海岸带所硕士研究生宋一晓和苏州大学博士研究生叶子凡为共同第一作者,烟台海岸带所王义鹏研究员为通讯作者。该研究得到国家自然科学基金、江苏省社会发展重点研发计划等项目支持。
文章信息:
Yixiao Song,Zifan Ye,Yipeng Wang. Metabolite-driven reprogramming of bacterial persisters: Mechanisms and therapeutic opportunities for overcoming antibiotic tolerance. Drug Resist Update. 2026,84:101322. https://doi.org/10.1016/j.drup.2025.101322
附件下载: